Введение
Кровь – наиболее дифференцированная и реактивная соединительная ткань. Являясь внутренней средой организма, представляет собой совокупность специализированных клеток и обеспечивает выполнение важнейших физиологических функций. У рептилий доля периферической крови составляет приблизительно 5–7 % от массы тела (Павлов, Юсупов, 2015). С наличием в крови белых кровяных телец (лейкоцитов) связана специфическая (адаптивный иммунитет), неспецифическая (в первую очередь фагоцитоз) защита организма, уровень стрессового воздействия (Davis et al., 2008). Измерение количественного соотношения лейкоцитарных клеток в крови животных позволяет оценить не только физиологическое состояние организма, но и его адаптивный потенциал (Хамидов и др., 1978; Чернышова, Старостин, 1994; Coico et al., 2003; Силс, 2008; Минеева, Минеев, 2011 и др.), а также получить сравнительные гематологические характеристики популяций рептилий в условиях антропогенного стресса.
Целью работы являлось изучение лейкоцитарной формулы крови гадюки обыкновенной Vipera berus (Linnaeus, 1758) из популяций в Самарской области.
Материалы
Отлов гадюк (68 особей) проводили в правобережной (Национальный парк «Самарская Лука», 19 особей) и левобережной (г. Самара, 49 особей) популяциях в 2013–2014 гг. (табл. 1).
Таблица 1. Время и места отлова гадюк
| Время отлова | Места отлова | Самки | Самцы |
| Июль 2013 г. | Волжский район Самарской области, Национальный парк «Самарская Лука» в окрестностях с. Шелехметь (естественного происхождения, особо охраняемая зона национального парка, редко посещаемая отдыхающими и рыбаками) | 5 | 14 |
| Май 2014 г. | Красноглинский район г. Самары (лесопарковая городская зона, часто посещаемая отдыхающими и спортсменами) | 13 | 6 |
| Июль 2014 г. | 14 | 2 | |
| Сентябрь 2014 г. | 3 | 11 | |
| Всего | 35 | 33 | |
Методы
Кровь брали пункцией иглой, смоченной в гепарине, из верхнечелюстной вены. После этого змей возвращали в место отлова. От каждой особи готовили мазки крови общепринятым гематологическим методом (окраска по Романовскому – Гимзе). Готовые мазки просматривали с иммерсией при увеличении ×1500.
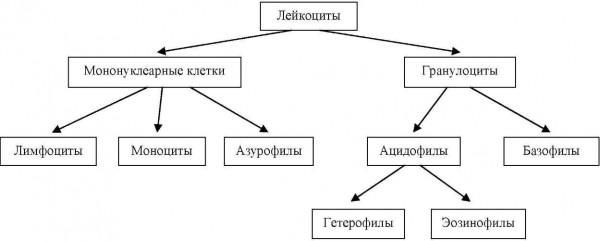
Мононуклеарные клетки дифференцировали на азурофилы, моноциты и лимфоциты. Гранулоциты разделяли на две группы: ацидофилы и базофилы, дополнительно выделяя гетерофилы и эозинофилы, отличающиеся друг от друга формой и цветом гранул (рис. 1).
Рис. 1. Классификация клеток лейкоцитарного ряда клеток рептилий (по: Coico et al., 2003; Arican, Cicek, 2010; Zimmerman et al., 2010; Лисничая, Ефимов, 2014 и др.)
Fig. 1. Classification of reptiles white blood cells (according to: Coico et al., 2003; Arican, Cicek, 2010; Zimmerman et al., 2010; Lisnichaya, Efimov, 2014, et al.)
На основании подсчета лейкоцитарной формулы рассчитывали индекс сдвига лейкоцитов крови как отношение суммы гранулоцитов к сумме агранулоцитов.
Цифровое изображение лейкоцитарных клеток крови выполнено камерой Vision CAM для тринокулярного микроскопа Meiji Techno с использованием интегрированного адаптера и разъема C-mount (увеличение ×1500).
Полученные экспериментальные данные обрабатывали с учетом нормальности распределения данных непараметрическим методом с расчетом критериев Манна – Уитни, Дана, Спирмана в пакете прикладных программ «Statistica». За величину статистической значимости принимали a = 0.05.
Результаты
Количественная оценка (%) основных видов лейкоцитарных клеток (формула крови, или лейкограмма) основана на распознавании образа клеток за счет различия их внешнего вида. Классификация лейкоцитов рептилий затруднена: частично за счет вариабельности строения клеток у разных видов, частично из-за присутствия большого количества незрелых форм, а также из-за отсутствия единой номенклатуры в литературе и проведения исследования клеточного состава крови различными, несогласованными методиками (Соколина и др., 1997). В целом лейкоциты рептилий можно разделить на две большие группы: гранулоциты и мононуклеары, то есть имеющие сегментированное и несегментированное ядро клетки. Гранулоциты можно разделить на две группы по цвету, в который окрашивается их цитоплазма в мазках крови по Романовскому – Гимзе: ацидофилы (розовый) и базофилы (фиолетовый). Ацидофилы, в свою очередь, делятся на гетерофилы и эозинофилы, отличающиеся друг от друга формой и цветом гранул.
Гетерофилы – это крупные (10–23 мкм) округлые клетки с бесцветной цитоплазмой, содержащей эозинофильные (оранжевые) палочко- или веретенообразные гранулы, преломляющие свет (Saint Girons, 1970). Края клеток могут быть неровными, в некоторых ситуациях можно даже наблюдать псевдоподии (ложноножки). Ядро зрелого гетерофила располагается эксцентрично, имеет округлую или овальную форму с глыбками концентрированного хроматина (рис. 2). Эозинофилы (рис. 3) – это крупные (11–17 мкм) округлые клетки со светло-синей цитоплазмой, округлым или овальным ядром, расположенным эксцентрично, и большим количеством округлых эозинофильных цитоплазматических гранул (Arikan, Cicek, 2014).
Базофилы (рис. 4), лимфоциты (рис. 5) и моноциты (рис. 6) крови рептилий схожи с таковыми у млекопитающих и птиц. Что касается дифференцировки у рептилий мононуклеарных клеток, то все исследователи выделяют моноциты и лимфоциты. Кроме того, у чешуйчатых, крокодилов и черепах в отдельный класс мононуклеаров выносят азурофилы (Martinez-Silvestre et al., 2005; Хайрутдинов, Соколина, 2010; Stacy et al., 2011). Азурофилы описаны как клетки нерегулярной формы (Frye, 1991). Ядро у них несегментированное, имеет неправильную округлую, овальную или двудольчатую форму. Хроматин ядра имеет зернистый вид. Цитоплазма базофильная, темнее, чем у моноцитов, окрашивается в интенсивный синий цвет, в ней присутствует небольшое количество матовых азурофильных гранул (Campbell, 2006) (рис. 7). Надо отметить, что существует и альтернативное мнение ряда авторов, полагающих, что моноциты и азурофилы рептилий по сути являются одним типом клеток (Veterinary..., 2012).

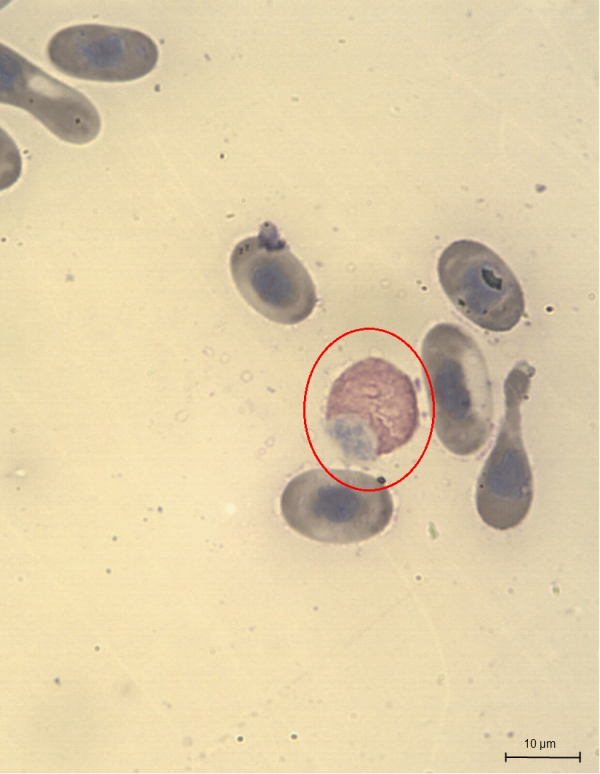
Рис. 2. Гетерофилы гадюки обыкновенной
Fig. 2. Heterophils of Vipera berus
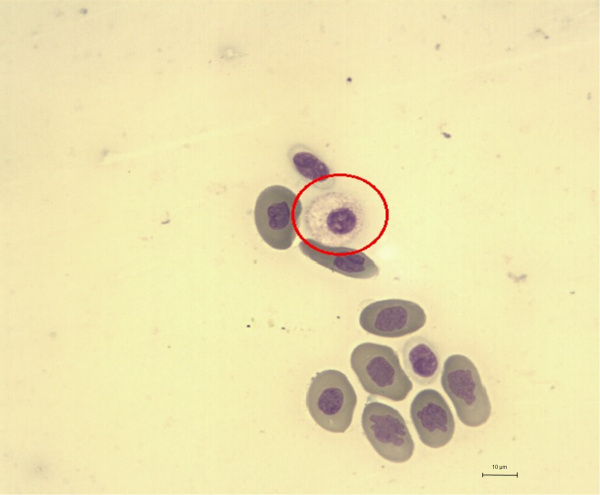
Рис. 3. Эозинофил гадюки обыкновенной
Fig. 3. Eosinophil of Vipera berus
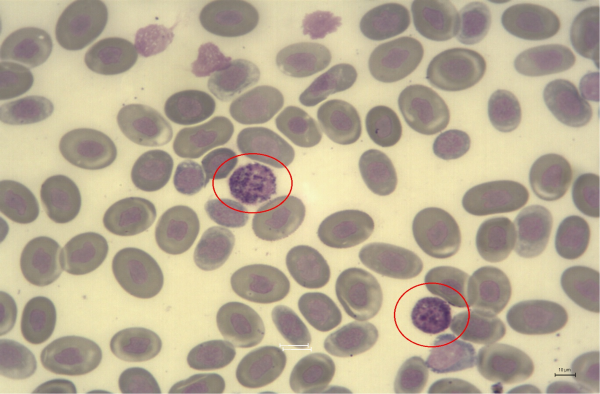
Рис. 4. Базофилы гадюки обыкновенной
Fig. 4. Basophils of Vipera berus
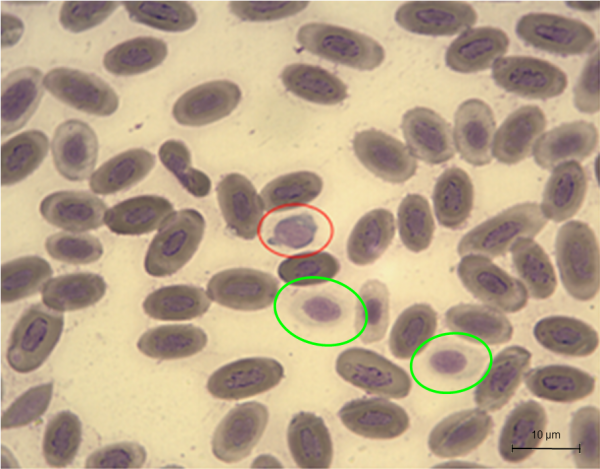
Рис. 5. Лимфоцит (красный цвет) и тромбоциты (зеленый цвет) гадюки обыкновенной
Fig. 5. Lymphocyte (red color) and thrombocytes (green color) of Vipera berus
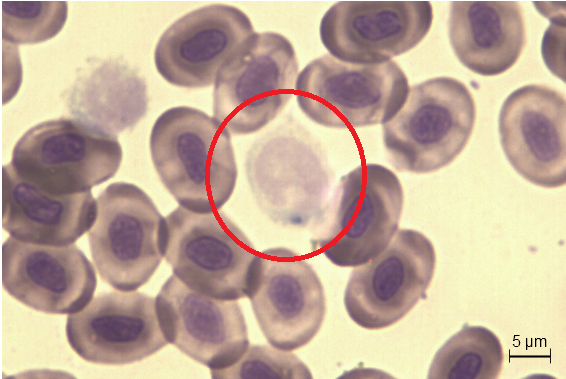
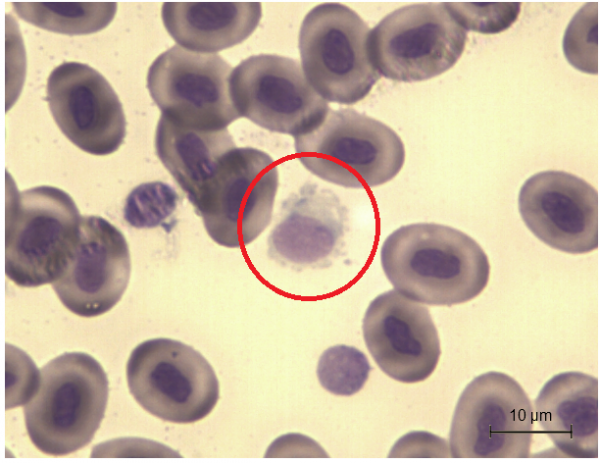
Рис. 6. Моноциты гадюки обыкновенной
Fig. 6. Monocytes of Vipera berus
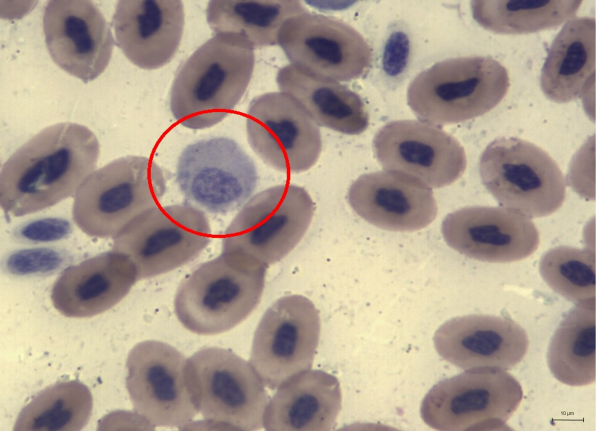
Рис. 7. Азурофил гадюки обыкновенной
Fig. 7. Azurophils of Vipera berus
С учетом анализа сведений литературы и собственных данных, в приготовленных мазках крови гадюки обыкновенной была проведена дифференцировка следующих клеток: среди гранулоцитов выделяли гетерофилы, эозинофилы и базофилы, среди агранулоцитов – азурофилы, моноциты и лимфоциты.
У самок и самцов гадюки обыкновенной, отловленных в Национальном парке «Самарская Лука», различий между полами в содержании форменных элементов в крови не выявлено (табл. 2).
Таблица 2. Лейкоцитарная формула периферической крови гадюки обыкновенной из Национального парка «Самарская Лука»
| Показатель лейкограммы | Самцы (n = 14) | Самки (n = 5) | Критерий Манна – Уитни (u, a) |
| Гетерофилы, % | 11.14 ± 0.40 | 10.20 ± 1.01 | 1.29, 0.19 |
| Эозинофилы, % | 9.14 ± 0.31 | 9.00 ± 0.89 | 0.37, 0.71 |
| Базофилы, % | 6.71 ± 0.54 | 6.60 ± 1.02 | 0.37, 0.70 |
| Азурофилы, % | 9.78 ± 0.60 | 9.00 ± 0.83 | 0.51, 0.61 |
| Моноциты, % | 12.71 ± 0.69 | 13.60 ± 1.77 | 0.37, 0.71 |
| Лимфоциты, % | 50.57 ± 1.08 | 51.20 ± 2.51 | 0.23, 0.81 |
| Индекс сдвига лейкоцитов, отн. ед. | 0.34 ± 0.01 | 0.32 ± 0.03 | 1.01, 0.31 |
Самки (табл. 3) и самцы (табл. 4) гадюки обыкновенной, отловленные в разное время 2014 г. в Самаре, также не различались по лейкоцитарному составу крови.
Таблица 3. Лейкоцитарный состав периферической крови самок гадюки обыкновенной из г. Самары
| Показатель лейкограммы | Время отлова | Критерий Манна – Уитни (u, a) | |
| май 2014 г. (n = 13) | июль и сентябрь 2014 г. (n = 17) | ||
| Гетерофилы, % | 8.07 ± 1.02 | 9.11 ± 0.75 | 0.83, 0.40 |
| Эозинофилы, % | 8.23 ± 0.62 | 7.23 ± 0.65 | 1.07, 0.29 |
| Базофилы, % | 4.53 ± 0.67 | 3.52 ± 0.62 | 1.08, 0.28 |
| Азурофилы, % | 12.69 ± 0.87 | 12.94 ± 0.85 | 0.19, 0.84 |
| Моноциты, % | 6.07 ± 0.74 | 7.88 ± 0.81 | 1.58, 0.12 |
| Лимфоциты, % | 60.38 ± 1.37 | 59.29 ± 1.39 | 0.54, 0.58 |
| Индекс сдвига лейкоцитов, отн. ед. | 0.27 ± 0.02 | 0.25 ± 0.02 | 0.52, 0.60 |
Таблица 4. Лейкоцитарный состав периферической крови самцов гадюки обыкновенной из г. Самары
| Показатель лейкограммы | Время отлова | Критерий Манна – Уитни (u, a) | |
| май 2014 г. (n = 6) | июль, сентябрь 2014 г. (n = 13) | ||
| Гетерофилы, % | 10.00 ± 1.17 | 8.30 ± 0.81 | 1.15, 0.26 |
| Эозинофилы, % | 8.16 ± 0.80 | 8.00 ± 0.80 | 0.12, 0.90 |
| Базофилы, % | 4.33 ± 0.94 | 4.30 ± 0.77 | 0.01, 0.98 |
| Азурофилы, % | 10.50 ± 1.03 | 12.15 ± 0.83 | 1.16, 0.26 |
| Моноциты, % | 5.33 ± 0.63 | 7.46 ± 0.73 | 1.84, 0.08 |
| Лимфоциты, % | 61.66 ± 0.90 | 59.76 ± 1.64 | 0.76, 0.45 |
| Индекс сдвига лейкоцитов, отн. ед. | 0.29 ± 0.02 | 0.26 ± 0.02 | 0.79, 0.43 |
При сравнении лейкоцитарных формул установлено перераспределение соотношения мононуклеарных клеток, выражающееся в возрастании доли азурофилов (u = 2.28, a = 0.02), лимфоцитов (u = 2.61, a = 0.008), и снижение доли моноцитов (u = 2.92, a = 0.003) (табл. 5) в крови самок гадюк из г. Самары по отношению к самкам из Национального парка «Самарская Лука».
Таблица 5. Лейкоцитарный состав периферической крови самок гадюки обыкновенной из Самарской области
| Показатель лейкограммы | Место отлова | Критерий Манна – Уитни (u, a) | |
| Национальный парк «Самарская Лука» (n = 5) | г. Самара (n = 30) | ||
| Гетерофилы, % | 10.20 ± 1.01 | 8.66 ± 0.61 | 0.84, 0.39 |
| Эозинофилы, % | 9.00 ± 0.89 | 7.66 ± 0.46 | 1.06, 0.28 |
| Базофилы, % | 6.60 ± 1.02 | 3.96 ± 0.46 | 1.93, 0.05 |
| Азурофилы, % | 9.00 ± 0.83 | 12.83 ± 0.60 | 2.28, 0.02 |
| Моноциты, % | 13.60 ± 1.77 | 7.10 ± 0.58 | 2.92, 0.003 |
| Лимфоциты, % | 51.20 ± 2.51 | 59.76 ± 0.97 | 2.61, 0.008 |
| Индекс сдвига лейкоцитов, отн. ед. | 0.32 ± 0.03 | 0.26 ± 0.01 | 1.79, 0.07 |
Примечание. Жирным шрифтом выделены статистически значимые различия.
Для самцов гадюки обыкновенной исследованных выборок различия были более выраженными и затрагивали кроме агранулоцитов и гранулоцитарный росток гемопоэза, о чем свидетельствовало снижение доли гетерофилов (u = 2.16, a = 0.03) и базофилов (u = 2.44, a = 0.01) в крови гадюки обыкновенной из г. Самары (табл. 6). Показатель индекса сдвига лейкоцитов у самцов самарского левобережья оказался статистически значимо ниже аналогичного показателя для правобережной популяции. Известно, что лейкоцитарный индекс характеризует степень выраженности эндоинтоксикации и свидетельствует о напряженности компенсаторных процессов в организме. Снижение этого показателя может быть в самом простом случае связано с возрастанием в крови доли агранулоцитов и активацией защитных процессов в организме, обусловленных в определенной мере уровнем антропогенного воздействия. С другой стороны, это свидетельствует о различиях в механизмах адаптации рептилий к среде обитания, что требует дальнейшего детального изучения.
Таблица 6. Лейкоцитарный состав периферической крови самцов гадюки обыкновенной из Самарской области
| Показатель лейкограммы | Место отлова | Критерий Манна – Уитни (u, a) | |
| Национальный парк «Самарская Лука» (n = 14) | г. Самара (n = 19) | ||
| Гетерофилы, % | 11.14 ± 0.40 | 8.84 ± 0.69 | 2.16, 0.03 |
| Эозинофилы, % | 9.14 ± 0.31 | 8.05 ± 0.61 | 1.18, 0.23 |
| Базофилы, % | 6.71 ± 0.54 | 4.32 ± 0.63 | 2.44, 0.01 |
| Азурофилы, % | 9.78 ± 0.60 | 11.63 ± 0.67 | 1.78, 0.07 |
| Моноциты, % | 12.71 ± 0.69 | 6.79 ± 0.57 | 4.42, 0.00001 |
| Лимфоциты, % | 50.57 ± 1.08 | 60.37 ± 1.15 | 4.33, 0.000015 |
| Индекс сдвига лейкоцитов, отн. ед. | 0.34 ± 0.01 | 0.27 ± 0.02 | 3.09, 0.001 |
Примечание. Жирным шрифтом выделены статистически значимые различия.
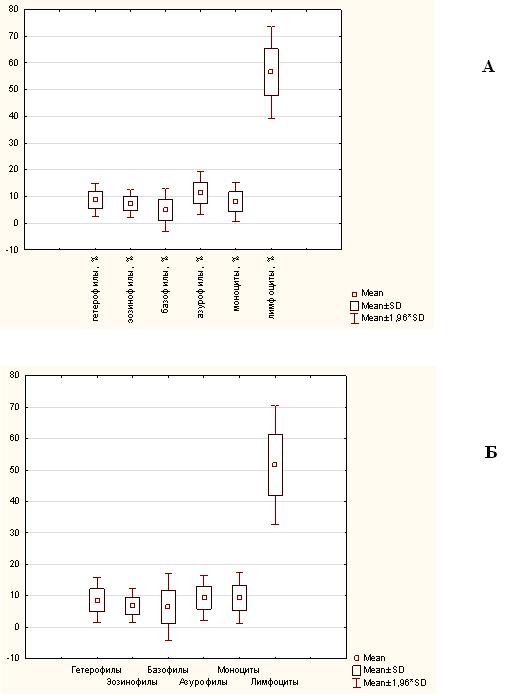
В целом можно заключить, что мононуклеарные клетки в лимфоцитарно-гранулоцитарном составе периферической крови обыкновенной гадюки из Самарской области составляли 70–80 %; из них лимфоциты у самок – 56.50 ± 1.34 %, самцов – 51.59 ± 1.27 %, моноциты у самок – 8.00 ± 0.57 %, самцов – 9.33 ± 0.54 %, азурофилы у самок – 11.33 ± 0.62 %, самцов – 9.43 ± 0.48 %. Доля гранулоцитов составляла 20–25 %, из них гетерофильных у самок – 8.69 ± 0.49 %, самцов – 8.64 ± 0.48 %, эозинофильных у самок – 7.42 ± 0.40 %, самцов – 6.85 ± 0.36 %, базофильных у самок – 4.95 ± 0.62 %, самцов – 6.52 ± 0.70 %. Диаграмма диапазонов («коробочный график») наглядно демонстрирует сразу несколько параметров распределения клеток: центральные тенденции (среднее значение), характеристики рассеяния (минимальное и максимальное значения), – и свидетельствует о долевом преобладании лимфоцитов в крови гадюки обыкновенной (рис. 8).
Рис. 8. Распределение количественных показателей лейкоцитарного состава периферической крови самок (А) и самцов (Б) гадюки обыкновенной из Самарской области: по оси ординат – доля клеток (%), по оси абсцисс – вид лейкоцитов
Fig. 8. The quantitative leucocyte composition distribution in peripheral blood of female (A) and male (B) Vipera berus from Samarskaya Oblast: y-axis - the proportion of cells (%), x-axis - the kind of white blood cells
Методом многомерного дисперсионного анализа было проведено сравнение по усредненным лейкоцитарным показателям выборок гадюки обыкновенной, различающихся по ряду факторов (полу, сезону, месту обитания). Полученное значение лямбды Уилкса (λWilks = 0.372, р < 0.001) свидетельствовало о значимости различий по совокупности показателей лейкоцитарного состава крови между выборками охраняемой территории (Национальный парк «Самарская Лука») и урбанизированной территории (г. Самара).
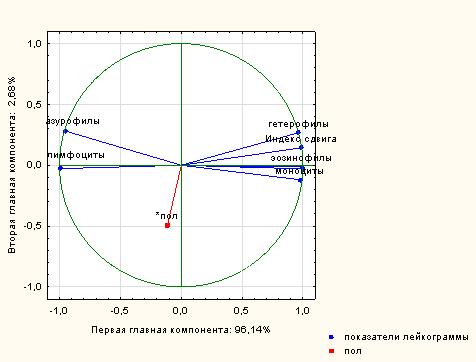
По результатам лейкоцитарного состава крови был проведен анализ исследованных выборок из популяций гадюки обыкновенной методом главных компонент. При помощи графика каменистой осыпи были выделены две компоненты (два фактора) с качеством репрезентации 98.8 %. Первая главная компонента, соответствующая максимальному собственному значению (6.73), описывает приблизительно 96.14 % общей вариации. Вторая компонента (0.18) описывает 2.68 % общей вариации. В первую главную компоненту наибольший вклад вносят эозинофилы (0.992), базофилы (0.999), гетерофилы (0.962), моноциты (0.977) и индекс сдвига лейкограммы (0.988). Вклад во вторую главную компоненту наиболее сильно коррелирует с содержанием азурофилов (0.281) (рис. 9).
Рис. 9. График факторных координат, построенный на основе лейкоцитарных показателей крови гадюки обыкновенной
Fig. 9. Graph of factor coordinates based on the quantitative leucocyte composition of Vipera berus
График распределения исследованных выборок гадюки обыкновенной в пространстве двух главных компонент (рис. 10) визуализирует полученный результат. По первой главной компоненте популяция урбанизированной территории (г. Самара) противостоит популяции охраняемой территории (Национальный парк «Самарская Лука»). Гадюка обыкновенная охраняемой территории занимает первый (самцы) и четвертый (самки) квадранты. Гадюка обыкновенная урбанизированной территории – второй (самки) и третий (самцы) квадранты. Различия по полу выражены гораздо слабее, чем по местообитанию.
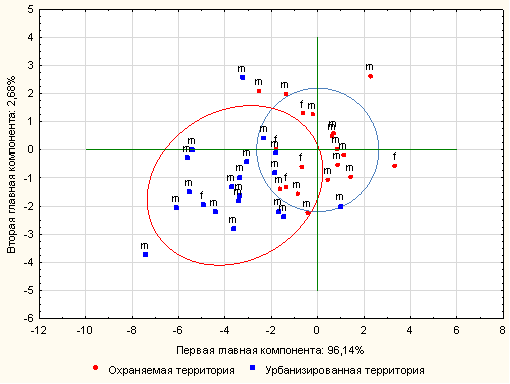
Рис. 10. Распределение выборок гадюки обыкновенной охраняемой и урбанизированной территорий (m – самцы, f – самки)
Fig. 10. Distribution of Vipera berus samples from the protected and urbanized areas (m – males, f – females)
Исследование линейной связи 15 анализируемых пар показателей лейкограммы корреляционным методом Спирмана (r) выявило различия в существовании и силе корреляционных взаимосвязей у самцов и самок гадюки обыкновенной. У самцов наличие статистически значимой корреляции установлено только в паре «базофилы – лимфоциты», показывающее, что возрастание доли лимфоцитов согласовано со снижением доли базофилов в периферической крови (табл. 7).
Таблица 7. Результаты корреляционного анализа для лейкоцитарных формул самцов гадюки обыкновенной (r, a)
| Вид лейкоцитов | Гетерофилы | Эозинофилы | Базофилы | Азурофилы | Моноциты | Лимфоциты |
| Гетерофилы | – | -0.08, 0.718 | 0.04, 0.971 | -0.08, 0.735 | -0.15, 0.530 | -0.45, 0.052 |
| Эозинофилы | -0.08, 0.718 | – | -0.19, 0.415 | -0.13, 0.588 | -0.13, 0.590 | -0.23, 0.343 |
| Базофилы | 0.04, 0.971 | -0.19, 0.415 | – | 0.001, 0.995 | 0.06, 0.785 | -0.50, 0.0288 |
| Азурофилы | -0.08, 0.735 | -0.13, 0.588 | 0.001, 0.995 | – | -0.21, 0.368 | -0.35, 0.138 |
| Моноциты | -0.15, 0.530 | -0.13, 0.590 | 0.06, 0.785 | -0.21, 0.368 | – | -0.24, 0.314 |
| Лимфоциты | -0.45, 0.052 | -0.23, 0.343 | -0.50, 0.0288 | -0.35, 0.138 | -0.24, 0.314 | – |
Примечание. Жирным шрифтом выделена статистически значимая корреляция.
Для самок гадюки обыкновенной число коррелирующих пар показателей было больше (3 из 15): лимфоциты – базофилы; лимфоциты – азурофилы; лимфоциты – моноциты. Таким образом, у самок гадюки возрастание доли лимфоцитов в крови было согласовано не только со снижением доли базофилов (r = -0.41, R2 = 0.16, p = 0.022), но и мононуклеарными клетками: азурофилами (r = -0.50, R2 = 0.25, p = 0.005) и моноцитами (r = -0.56, R2 = 0.31, p = 0.001) (табл. 8).
Таблица 8. Результаты корреляционного анализа для лейкоцитарных формул самок гадюки обыкновенной (r, a)
| Вид лейкоцитов | Гетерофилы | Эозинофилы | Базофилы | Азурофилы | Моноциты | Лимфоциты |
| Гетерофилы | – | -0.33, 0.074 | 0.01, 0.921 | -0.36, 0.05 | -0.09, 0.622 | -0.20, 0.289 |
| Эозинофилы | -0.33, 0.074 | – | -0.08, 0.642 | -0.06, 0.741 | -0.32, 0.078 | -0.06, 0.724 |
| Базофилы | 0.01, 0.921 | -0.08, 0.642 | – | -0.12, 0.514 | 0.08, 0.65 | -0.41, 0.022 |
| Азурофилы | -0.36, 0.05 | -0.06, 0.741 | -0.12, 0.514 | – | 0.23, 0.221 | -0.50, 0.005 |
| Моноциты | -0.09, 0.622 | -0.32, 0.078 | 0.08, 0.65 | 0.23, 0.221 | – | -0.56, 0.001 |
| Лимфоциты | -0.20, 0.289 | -0.06, 0.724 | -0.41, 0.022 | -0.50, 0.005 | -0.56, 0.001 | – |
Примечание. Жирным шрифтом выделена статистически значимая корреляция.
Заключение
Известно, что наличие корреляции между показателями вовсе не означает обязательной причинно-следственной связи между ними, и биологическая интерпретация установленных отношений связана с более выраженной у самок гадюк активацией адаптивного иммунитета. Для поддержания гомеостаза организма при действии различных стрессовых факторов среды (биотических и антропогенных) и самки, и самцы используют универсальный набор эффекторных клеток, среди которых азурофилы, моноциты, гетерофилы, базофилы и эозинофилы. Это компоненты врожденных иммунных реакций (Coico et al., 2003; Davis et al., 2008), они действуют, чтобы ограничить распространение инфекции, и активируют клетки адаптивного иммунитета, в первую очередь лимфоциты. Другими словами, реакции врожденного иммунитета создают условия для развертывания клеточно-опосредованного или гуморального адаптивного иммунитета, формирующегося при участии лимфоцитов. Для гадюки обыкновенной из левобережной популяции (лесопарковая зона г. Самары), по сравнению с правобережной популяцией (Национальный парк «Самарская Лука»), выявлено возрастание доли основных клеток агранулоцитарного ряда (азурофилов и лимфоцитов), свидетельствующее о повышении защитной функции крови. Установленные особенности лейкоцитарного состава связаны как с популяционно-генетическими особенностями, так и со спецификой среды обитания, накладывающей отпечаток на физиологическое состояние рептилий.
Библиография
Лисничая Е. Н., Ефимов В. Г. Особенности исследования морфологического состава крови рептилий // Науково-технiчний бюлетень НДЦ бiобезпеки та екологiчного контролю ресурсiв АПК. 2014. Т. 2. № 1. С. 61–74. URL: http://nbuv.gov.ua/j-pdf/ndbnndc_2014_2_1_11.pdf (дата обращения 22.03.2016).
Минеева О. В., Минеев А. К. Нарушения лейкоцитарной формулы крови озерной лягушки Саратовского водохранилища // Вестн. Нижегород. ун-та им. Н. И. Лобачевского. 2011. № 2. С. 94–97.
Павлов А. В., Юсупов Р. Х. Система крови // Бакиев А. Г., Гаранин В. И., Гелашвили Д. Б. и др. Гадюки (Reptilia: Serpentes: Viperidae: Vipera) Волжского бассейна. Ч. 1 . Тольятти: Кассандра, 2015. С. 137–155.
Силс Е. А. Сравнительный анализ гематологических показателей остромордой (Rana arvalis, Nilsson, 1842) и озерной (Rana ridibunda, Pallas, 1771) лягушек городских популяций // Вестн. Оренбург. ун-та. 2008. № 10 (92). С. 230–235.
Соколина Ф. М., Павлов А. В., Юсупов Р. Х. Гематология пресмыкающихся: Методическое пособие к курсу герпетологии, большому практикуму и семинарам . Казань: Казан. ун-т, 1997. 31 с.
Хайрутдинов И. З., Соколина Ф. М. Характеристика крови рептилий и ее связь с условиями среды обитания . Казань: Казан. ун-т, 2010. 44 с.
Хамидов Д. Х., Акимов А. Т., Турдыев А. А. Кровь и кроветворение у позвоночных животных . Ташкент: Фан, 1978. 168 с.
Чернышова Э. В., Старостин В. И. Периферическая кровь лягушек рода Rana как тест-система для оценки загрязнения окружающей среды // Изв. РАН. 1994. Сер. биол. № 4. С. 656–660.
Arican H., Cicek K. Morphology of peripheral blood cells from various species of Turkish Herpetofauna // Acta Herpetologica. 2010. Vol. 5. № 2. P. 179–198.
Arican H., Cicek K. Haematology of amphibians and reptiles: a review // North-Western journal of zoology. 2014. Vol. 10. № 1. P. 190–209. URL: http://biozoojournals.ro/nwjz/index.html (дата обращения 22.03.2016).
Campbell T. W. Clinical pathology of reptiles // Reptile medicine and surgery. 2nd edition. St. Louis (MO): Saunders Publishing, 2006. P. 453–470.
Coico R., Sunshine G., Benjamini E. Immunology: A Short Course. Hoboken; NJ: Wiley-Liss Publications, 2003. 500 p.
Davis F. R., Maney D. L., Maers J. C. The use of leukocyte profiles to measure stress in vertebrates: a review for ecologists // Functional Ecology. 2008. Vol. 22. P. 760–772.
Frye F. L. Hematology as applied to clinical reptile medicine // Biomedical and surgical aspect of captive reptile husbandry. Vol. 1. Malabar, Florida: Krieger Publishing Co., 1991. P. 209–280.
Martinez-Silvestre A., Marco I., Rodriguez-Dominguez M. A., Lavin S., Cuenca R. Morphology, cytochemical staining, and ultrastructural characteristics of blood cells of the giant lizard E1 Hierro (Gallotia simonyi) // Research in Veterinary Science. 2005. Vol. 78. P. 127–134.
Saint Girons M. C. Morphology of the circulating blood cells // Biology of Reptilia. Vol. 3. London; New York: Academic Press, 2005. 1970. P. 73–91.
Stacy N., Alleman A. R., Sayler F. Diagnostic Hematology of Reptiles // Clin. Lab. Med. 2011. Vol. 31. P. 87–108.
Veterinary Hematology and Clinical Chemistry. 2nd edition. Wiley-Blackwell, 2012. 776 p.
Zimmerman L. M., Vogel L. A., Bowden R. M. Understanding the vertebrate immune system: insights from the reptilian perspective // J. Exp. Biol. 2010. Vol. 213. P. 661–671.
Благодарности
Авторы выражают признательность А. В. Павлову (Волжско-Камский заповедник) за ценные замечания.






 © 2011 - 2026
© 2011 - 2026