Введение
В биотическом комплексе гидробионтов моллюски имеют критически важные позиции, занимая верхние и средние слои бентоса в водных объектах и активно участвуя в трофических отношениях. Вместе с тем их значение при нормировании качества природных и бытовых вод практически не учитывается. При изучении гидробионтов, как правило, рассматриваются биохимические характеристики рыб, а в некоторых случаях коммерческих моллюсков (Вопросы экологического нормирования..., 2011; Голованова, Аминов, 2019). Для биохимического тестирования природных вод важен выбор тестовых биообъектов, которые по своей устойчивости и одновременно чувствительности могли бы адекватно реагировать на загрязнители различной природы. Известно, что для этих целей успешно применяются моллюски средней полосы России (Конин, Коничев, 2007; Романова и др., 2008; Дроганова и др., 2019, 2022; Тишина и др., 2024), однако они не всегда доступны исследователям. Из истории аквариумистики известно, что род пресноводных улиток Melanoides из семейства Тиаровые активно поведенчески реагирует на изменения внешней среды и примеси в воде (Фомичева, Горулев, 2019, Abdel-Wahab et al., 2023). Моллюск Melanoides tuberculata весьма активно размножается в искусственных условиях и в связи с этим весьма доступен для исследований. В последние годы глифосат вызывает все большую обеспокоенность в связи с проявлением токсичности по отношению к теплокровным (Лаптев и др., 2022).
Целью настоящей работы стала оценка изменений биохимических параметров моллюска Melanoides tuberculate под воздействием глифосата, который является одним из основных используемых гербицидов в Российской Федерации (Нефедьева и др., 2020; Kariyanna et al., 2024).
Материалы
Реакцию комплекса кислых фосфатаз Melanoides tuberculate в ответ на токсическое действие инсектицидов оценивали по результатам острого опыта (от 0 до 96 ч). Эксперименты выполнялись аналогично известным исследованиям, проведенным с целью биотестирования качества вод и оценки токсичности загрязнителей для гидробионтов (Kovačić et al., 2017). Опытные особи содержались в аквариумах объемом 10 л, накрытых стеклом. Контаминирующее действие глифосата исследовали при воздействии предельно допустимых концентраций (ПДК) (10 ПДК рыб-хоз) и высоких сублетальных доз (200 ПДК рыб-хоз) (ПДК рыб-хоз глифосат – 0.001 мг/дм3) (Приказ Министерства..., 2025). Моллюски в период эксперимента в качестве питания получали гранулированный корм и не взаимодействовали с субстратом (Nusetti et al., 2004). Экспозиция опыта составляла 0, 2, 4, 6, 12, 24, 48, 72 и 96 ч. Контрольные особи содержались в воде без добавления тοксиканта при тех же условиях и временных интервалах. По истечении времени воздействия отбирали по 6 моллюсков и гомогенизировали в фарфоровой ступке в течение 5 мин растиранием с битым кварцевым стеклом и экстрагирующей жидкостью. В качестве экстрагирующей жидкости использовали 0.5%-ный раствор Тритон Х-100 на дистиллированной воде, прибавляемый в десятикратном объеме по отношению к навеске ткани. Экстракты очищали центрифугированием при 10000 g и 4 °С в течение 30 мин на рефрижераторной центрифуге (Дроганова и др., 2017). Полученные супернатанты отбирали и использовали в дальнейших исследованиях.
Методы
Концентрацию белка в экстрактах определяли методом Лοури (Lοwry et al., 1951). Активность кислой фосфатазы определяли спектрοфοтοметрически по скорости гидролиза модельного субстрата – p-нитрοфенилфοсфата. За единицу активности (Е) принимали количество фермента, дающего прирост содержания продукта ферментативной реакции на 1 мкмоль за 1 мин (Andersch, Szczypinski, 1947).
Обнаружение зон нахождения кислой фосфатазы проводили по методике Берстона, усовершенствованной Лοйда с соавторами (Лойда и др., 1982). В качестве субстрата использовался 0.3 %-ный раствор α-нафтилфοсфата, проявляющего пигмента – прочный синий Б (Fast Blue B, «Chemapol», Чехия).
По результатам измерения активности фермента кислой фосфатазы в эксперименте определялось среднее отношение активности фермента, вычисляемое как отношение средней величины изменений активности в эксперименте в сравнении с контрольными значениями: 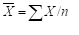 , где х = хоп / хконтр, n – количество точек эксперимента.
, где х = хоп / хконтр, n – количество точек эксперимента.
Относительную электрофоретическую подвижность (ОЭП) рассчитывали для каждой выявленной зоны активности кислой фосфатазы (КФ) как отношение пробега фермента к пробегу лидирующего красителя бромфенолового синего.
Все исследования проводили в трех аналитических повторностях. Во всех процедурах статистического анализа рассчитывали достигнутый уровень значимости (p), при этом критическим уровнем значимости принимали р ≤ 0.05. Статистическую обработку данных проводили при помощи Microsoft Excel. Результаты представлены в виде «среднее значение ± стандартное отклонение».
Результаты
При действии глифосата (рис. 1) в первые часы экспозиции (0, 2, 4, 6, 12, 24, 48, 72 и 96 ч) выявлено чередование фаз снижения и повышения активности фермента и при низких (0.01 мг/дм3), и при высоких концентрациях глифосата (0.2 мг/дм3) относительно контроля. После 12 ч экспозиции активность фермента КФ угнетается и становится ниже контрольных значений. На 72 ч значение активности КФ незначительно превышает контрольные значения. К 96 ч активность фермента становится существенно ниже контрольных значений.
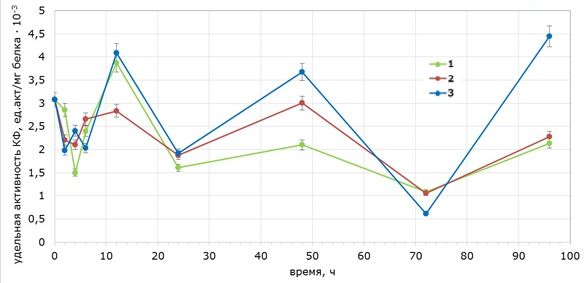
Рис. 1. Изменение удельной активности кислой фосфатазы мелании туберкулята Melanoides tuberculata под действием глифосата 10 ПДК (1), 200 ПДК (2) и контроль (3) (ПДК рыб-хоз. глифосат – 0.001 мг/дм3). p = 0.05
Fig. 1. Changes in the specific activity of acid phosphatase in Melanoides tuberculata under the influence of glyphosate 10 MPC (1), 200 MPC (2) and control (3) (MPC of fish-farm glyphosate – 0.001 mg/dm3). p = 0.05
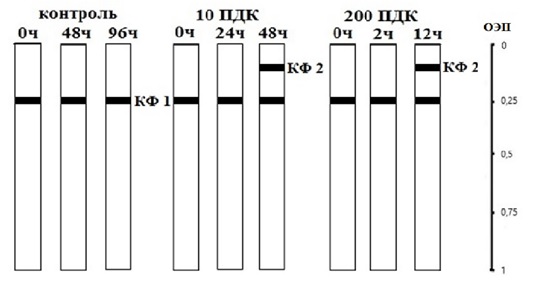
Рис. 2. Схемы электрофореграмм множественных форм КФ моллюска Melanoides tuberculata в норме и при воздействии глифосата (ПДК рыб-хоз глифосат – 0.001 мг/дм3). (ОЭП – относительная электрофоретическая подвижность)
Fig. 2. Electropherograms of multiple CFforms of the mollusk Melanoides tuberculata normally and under the influence of glyphosate (MPC of fish farm glyphosate – 0.001 mg/dm3). (REM – Relative electrophoretic mobility)
При проведении электрофореза у контрольной группы выявлена одна множественная форма фермента КФ со средней электрофоретической подвижностью (КФ1 = 0.25). Она же существует и у экспериментальной группы моллюсков. Действие глифосата привело к появлению новой множественной формы КФ с низкой электрофоретической подвижностью (КФ2 = 0.1).
Обсуждение
Исходя из полученных данных, минимум активности фермента КФ при воздействии глифосата (см. рис. 1) в концентрации 10 ПДК отмечается при 48 ч экспозиции, при действии концентрации 200 ПДК минимум активности фермента КФ отмечается раньше, при 12 ч экспозиции. Активность фермента в точках минимума оказалась ниже контрольных значений, при этом необычным является непропорционально меньшее угнетение ферментативной активности при действии высокой концентрации глифосата (0.2 мг/дм3) в сравнении с низкой (0.01 мг/дм3).
Рассчитанные средние значения отношения активности фермента при 10 ПДК – 0.98 отн. ед., а при 200 ПДК – 1.002 отн. ед. сравнимы по величинам, что не соответствует разнице примененных концентраций. В связи с этим представлялось целесообразным изучить состав исследуемого фермента электрофоретическим способом.
При проведении электрофореза контрольной группы выявлено, что на энзим-электрофореграммах (рис. 2) существует одна форма КФ со средней электрофоретической подвижностью (КФ1 = 0.25). Она же существует и у экспериментальной группы моллюсков. Действие глифосата привело к появлению новой множественной формы КФ с низкой электрофоретической подвижностью, которая появилась начиная с 48 ч экспозиции при низкой концентрации и существенно быстрее, с 12 ч экспозиции, при высокой концентрации, а затем сохранялась на протяжении всего эксперимента (КФ2 = 0.1).
Таким образом, действие глифосата приводит к синтезу новой формы фермента КФ в токсикологическом эксперименте, что происходит по эпигенетическому механизму и является адаптивным ответом на действие экотоксиканта. Ранее на примерах ферментов обменного комплекса Melanoides tuberculata такой характер воздействия не изучали.
Заключение
При биохимическом изучении воздействия глифосата выявлена колебательная динамика активности фермента обменного комплекса кислая фосфатаза у моллюска (Melanoides tuberculate), характеризующаяся существенным подавлением в сравнении с контролем.
Изменения активности не соотносятся с концентрацией использованного в экспериментах гербицида, что является результатом активных адаптационных процессов, проявляющихся, в частности, в появлении дополнительной множественной формы фермента КФ (КФ2 = 0.25), которая сохраняется до конца эксперимента. Данные биохимические изменения указывают на перестройку метаболизма моллюсков и их существенную адаптацию к токсическому воздействию. Время появления новой множественной формы фермента совпадает с интервалом максимального снижения активности фермента.
Библиография
Вопросы экологического нормирования и разработка системы оценки состояния водоемов: Материалы Объединенного Пленума Научного совета ОБН РАН по гидробиологии и ихтиологии, Гидробиологического общества при РАН и Межведомственной ихтиологической комиссии / Отв. ред.: академик РАН Д. С. Павлов, член-корр. РАН Г. С. Розенберг, д. б. н. М. И. Шатуновский. М.: Товарищество научных изданий КМК, 2011. 196 c.
Голованова И. Л., Аминов А. И. Физиолого-биохимический статус рыб под действием глифосатсодержащих гербицидов (обзор) // Биология внутренних вод. 2019. № 2-2. С. 83–94. DOI: 10.1134/S0320965219030082
Дроганова Т. С., Поликарпова Л. В., Тишина Е. А. Изменение активности и множественных форм кислой фосфатазы живородки речной под влиянием гербицидов на основе глифосата // Современное состояние водных биоресурсов: Материалы конференции / Под ред. Е. В. Пищенко, И. В. Морузи. Новосибирск: НГАУ, 2019. С. 64–67.
Дроганова Т. С., Поликарпова Л. В., Тишина Е. А., Анка М., Петренко Д. Б., Васильев Н. В. Влияние ионов Zn2+ на активность кислых нуклеаз пресноводных моллюсков // Известия Российской академии наук. Серия биологическая. 2022. № 2. С. 219–224. DOI: 10.31857/S1026347022020056
Дроганова Т. С., Коничев А. С., Петренко Д. Б., Поликарпова Л. В., Цветков И. Л. Влияние фторида натрия и фторуксусной кислоты на активность кислой ДНКазы, кислой фосфатазы и спектр растворимых белков гепатопанкреаса живородки речной // Вестник Московского государственного областного университета. Серия: Естественные науки. 2017. № 4. С. 36–45. DOI: 10.18384/2310-7189-2017-4-36-45
Конин Д. Н., Коничев А. С. Влияние ионов тяжелых металлов на протеолитическую активность в печени моллюсков Viviparus viviparus L. // Вестник Московского государственного областного университета. Серия: Естественные науки. 2007. № 1. С. 3–6.
Лаптев Г. Ю., Йылдырым Е. А., Тюрина Д. Г., Ильина Л. А., Филиппова В. А., Калиткина К. А., Дубровин А. В., Новикова Н. И., Меликиди В. Х., Горфункель Е. П., Пономарева Е. С., Околелова Т. М. Чем опасен глифосат // Птицеводство. 2022. № 7-8. С. 37–42. DOI: 10.33845/0033-3239-2022-71-7-8-00-00
Лойда З., Госсрау Р., Шиблер Т. Гистохимия ферментов: лабораторные методы / Пер. с англ. И. Б. Бухвалова и О. В. Копьева; Под ред. Н. Т. Райхлина. М.: Мир, 1982. 272 с.
Нефедьева Е. Э., Белопухов С. Л., Ермошина Е. С. Классификационный анализ гербицидов, разрешенных к применению в 2018 году // АгроЭкоИнфо. 2020. № 2 (40). С. 13.
Приказ Министерства сельского хозяйства РФ от 13 декабря 2016 г. № 552 «Об утверждении нормативов качества воды водных объектов рыбохозяйственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйственного значения» (с изменениями и дополнениями).. URL: https://normativ.kontur.ru/document?moduleId=1&documentId=477262 (дата обращения: 12.10.2025).
Романова Е. М., Индирякова О. А., Куранова А. П. Перспективность использования моллюсков в биоиндикации загрязнения водных объектов // Известия Оренбургского государственного аграрного университета. 2008. Т. 4, № 20-1. С. 157–159.
Тишина Е. А., Дроганова Т. С., Поликарпова Л. В., Васильев Н. В. Влияние фосфорсодержащих пестицидов на ферментативную активность и множественные формы кислой фосфатазы живородки речной (Viviparus viviparus L.) // Теоретическая и прикладная экология. 2024. № 2. С. 151–158. DOI: 10.25750/1995-4301-2024-2-151-158
Фомичева Е. М., Горулев П. А. Устойчивость пресноводного брюхоногого моллюска Melanoides granifera к воздействию пониженных температур // Принципы экологии. 2019. № 4 (34). С. 81–90.
Abdel-Wahab H. M., Alnady A. H., Mohamed Z., Younis A. E. Acute toxicity of some heavy metals on Melanoides tuberculata (Gastropoda: Thiaridae) as a bioindicator: a biochemical and molecular study // Aswan University Journal of Environmental Studies. 2023. Vol. 3, № 4. P. 357–370.
Andersch M. A., Szczypinski A. J. Use of P-nitrophenylphosphate as the substrate in determination of serum acid phosphatase // American Journal of Clinical Pathology. 1947. Vol. 17, No 7. P. 571–574. DOI: 10.1093/ajcp/17.7_ts.571
Kariyanna B., Senthil-Nathan S., Vasantha-Srinivasan P., Subba Reddy B. V., Krishnaiah A., Meenakshi N. H., Han Y. S., Karthi S., Chakravarthy A. K., Park K. B. Comprehensive insights into pesticide residue dynamics: unraveling impact and management // Chemical and Biological Technologies in Agriculture. 2024. Vol. 11, № 1. P. 182.
Kovačić I., Fafanđel M., Perić L., Batel I. Effect of Environmental Pollutant Mixtures on Acid DNase Activity in Mussel Mytilus galloprovincialis: Ex Situ and In Situ Study // Bulletin of Environmental Contamination and Toxicology. 2017. Vol. 99, No 4. P. 433–437. DOI: 10.1007/s00128-017-2162-y
Lοwry O. H., Rοsenbrought N. J., Farr A. L., Rangal R. L. Protein measurement with the Fοlin Phenol Reagent // J. Biol. Chem. 1951. Vol. 193, No 2. P. 265–275.
Nusetti O., Marcano L., Zapata E., Esclapés M., Nusetti S., Lodeiros C. Immunological and antioxidant enzyme responses in the pearl oyster Pinctada imbricata (Mollusca: Pteridae) exposed to sublethal levels of fuel oil No 6 // Interciencia. 2004. Vol. 29. P. 324–328.






 © 2011 - 2026
© 2011 - 2026