Введение
В гидросфере среди соединений серы сульфаты являются одним из важнейших анионов и присутствуют практически во всех поверхностных водах. В зависимости от истории образования водоема, формы озерной ванны, климатических условий, характера окружающих пород и гидрологического режима озера содержание этих ионов в воде может варьировать в широких пределах (Глобальный биохимический цикл…, 1983). В анаэробных условиях может протекать процесс, в котором сульфат используется сульфатредуцирующими бактериями (СРБ) в качестве конечного акцептора электронов при окислении органических веществ или водорода (Иванов, 1979; Глобальный биохимический цикл…, 1983; Волков, 1984; Вайнштейн, 1996). Схематически сущность процесса сульфатредукции отражается уравнением:
[С] + SO42- +6Н+ → Н2S + СО2 +2Н2О.
В результате данного процесса образуется сероводород. Особое внимание уделяется именно недиссоциированному соединению. Это связано с его большей токсичностью, в результате чего молекулярный сероводород представляет опасность для гидробионтов, в том числе и для серобактерий (Тимофеева, 1991). В кислой среде практически отсутствуют ионные формы сероводорода, поэтому данное соединение находится в растворенном состоянии в виде молекул. При повышении значения pH уменьшается количество растворенного молекулярного сероводорода и увеличивается доля ионизированных форм сульфид- и гидросульфид-ионов (Хатчинсон, 1969). В воде окисление сероводорода происходит в основном до элементной серы и сульфат-иона. В донных отложениях образующийся в результате бактериального восстановления сульфатов сероводород может связываться ионами металлов в малорастворимые сульфиды, которые, как и он сам, в дальнейшем трансформируется в различные соединения серы. Среди форм серы в донных отложениях (ДО) преимущественно встречаются: сульфидная (кислоторастворимые сульфиды), пиритная (дисульфид железа), элементная и сера, связанная с органическим веществом (Остроумов, 1953). Эти соединения входят в состав так называемой суммы производных сероводорода (∑SH2S). На интенсивность процесса сульфатредукции в основном могут оказывать влияние: содержание сульфатов, количественный и качественный состав органического вещества (ОВ), а на накопление форм серы – производных сероводорода − также и наличие реакционноспособного железа в среде (Волков, 1984). В проводимых нами ранее исследованиях на территории Архангельской области для мелководных низкоминерализованных озер (глубина до 8 м) Кенозерского национального парка было выявлено, что основным лимитирующим фактором протекания сульфатредукции в донных отложениях этих водоемов являются низкие концентрации сульфатов, не превышающие 2 мг/л как в водной толще, так и в жидкой фазе осадков. Общее количество соединений восстановленной серы в донных отложениях этих водоемов в среднем составляло 0.18 % а.с.в. (Титова, Кокрятская, 2018). Наибольшее содержание соединений восстановленной серы в осадках отмечалось в поверхностных слоях (до 10 см) с заметным снижением в их толще. Среди отмеченных форм серы в оба сезона доминирующей была органическая составляющая до 90 % ∑SH2S (Титова, Кокрятская, 2018). В изученных мелководных озерах Коношского района (Нижнее, Святое) с концентрациями сульфатов в воде (до 5 мг/л) и жидкой фазе отложений (до 2000 мг/л) соединений восстановленной серы накапливалось лишь немногим более − от 0.19 до 0.29 % а.с.в. Причиной этому служит недостаток органических веществ, доступных для СРБ, поскольку из-за небольшой глубины озер в аэробных условиях водной толщи поступившее в водоемы ОВ подвергается незначительной деструкции. Доминирующей формой среди соединений восстановленной серы оставалась органическая составляющая. В оз. Белое, отличающемся большими количествами сульфатов в воде (в среднем − до 12 мг/л, максимально − до 30 мг/л) и жидкой фазе отложений до 5000 мг/л, соединений восстановленной серы в ДО накапливалось заметно больше (в среднем до 2.40 % а.с.в.) и не наблюдалось заметного снижения этого параметра в толще отложений. Доминирующей формой среди соединений восстановленной серы в ДО становилась пиритная − от 50 до 90 % ∑SH2S (Титова и др., 2017).
Цель настоящей работы − изучение особенностей процесса сульфатредукции в оз. Назаровское по распределению форм серы и выявление его особенностей.
Материалы
Объектом нашего исследования являлось оз. Назаровское, расположенное в Коношском районе Архангельской области в подзоне средней тайги с умеренным континентальным климатом и относящееся к водосборному бассейну р. Онега (верхнему ее течению). Изучаемая территория расположена на высоком водораздельном массиве между реками Вагой и Онегой со сравнительно малой заболоченностью, где господствуют ельники-зеленомошники, а также ельники-черничники с примесью лиственных пород и сосны (Агроклиматический справочник…, 1961).
Оз. Назаровское (рис. 1) с площадью водной поверхности 0.325 км2 относится к категории малых водоемов (Драбкова, 1979). Длина достигает 1.86 км, максимальная ширина – 0.33 км, средняя глубина – 1.80 м, максимальная − 5 м (этот участок обозначен на схеме точкой и был выбран для отбора проб). По показателю условного водообмена озеро – сильноводообменное. Соединено ручьем с соседним оз. Белое, результаты изучения которого ранее были опубликованы (Титова и др., 2017).
Пробы воды отбирались в соответствии с (ГОСТ, 2000) послойно через 0.5 м на глубоководном участке (реперной станции) с помощью поликарбонатного горизонтального батометра вместимостью 2−5 л в зимний (март) и летний (июль) периоды. Пробы донных отложений отбирались согласно (ГОСТ, 1980) на той же станции, что и вода, с помощью ударной прямоточной грунтовой трубки с внутренним диаметром 50 мм, длиной 1 м (Aquatic Research Instruments) послойно с шагом 5 см (реже 1−2 см в основном для поверхностных горизонтов).
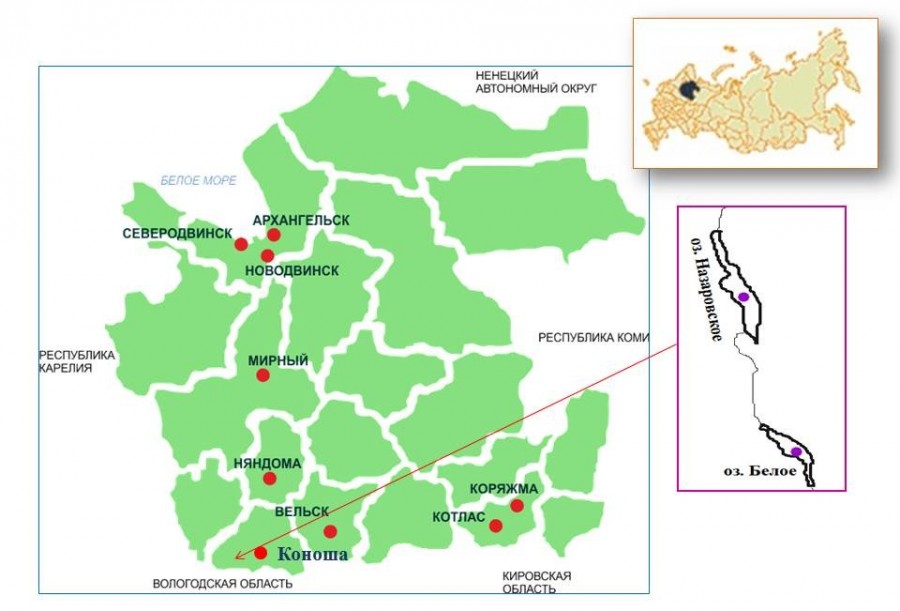
Рис. 1. Схема месторасположения оз. Назаровское
Fig. 1. Location of Lake Nazarovskoe
Методы
Определение сероводорода и сульфидов проводили фотометрическим методом с образованием метиленового синего в качестве конечного продукта (РД…, 2010). Определение сульфатов в воде проводилось хроматографически на жидкостном хроматографе LC-20 Prominence с кондуктометрическим детектором (ПНД ф, 2008). Растворенный органический углерод определялся на ТОС-анализаторе (ISO,1999). Определение концентраций растворенного железа в воде проводилось фотометрическим методом с образованием комплексного соединения его с феррозином, окрашенного в фиолетовый (пурпурный) цвет (Кононец и др., 2002). Определение различных форм серы в донных отложениях проводили по методике, разработанной в лаборатории геохимии Института океанологии им. П.П. Ширшова РАН (Волков, Жабина, 1980). Методика предусматривает определение сульфидной, элементной, пиритной и органической форм серы из одной навески донных осадков. Использовались титриметрические, фотометрические и гравиметрические методы анализа. Определение реакционноспособных форм железа проводили раздельно после извлечения их из осадка 3.5 N серной кислотой (Соколов, 1980). Определение общего и органического углерода и азота проводили методом сухого сжигания с последующим газохроматографическим разделением газовой смеси на C,H,N-анализаторе фирмы «Hewlett-Packard» (Гельман и др., 1987). Лабильное органическое вещество определялось по методике (Rovira, Vallejo, 2002). Интенсивность бактериальной сульфатредукции определялась радиоизотопным методом с использованием меченого по сере Na235SO4. Обработка результатов проводилась с помощью Excel 2010.
Результаты
Исследования озера Назаровское охватывают период с 2013 по 2017 г.
Гидрохимический состав воды отражен в формуле Курлова, где М − минерализация в мг/л; 1– март, 2 –июль.

Как видно из данных, приведенных выше, вода в озере пресная, гидрокарбонатного класса кальциевой группы. Минерализация в зимний и летний периоды отличается почти на 100 мг/л. Повышения минерализации вод зимой могли быть связаны как с разгрузкой грунтовых вод, так и с концентрированием солей в подледный меженной период. Вклад гидрокарбонатов в минеральный состав вод озера увеличивался от зимы к лету, а их содержание снижалось − от 124 до 65 мг/л в среднем.
При этом доля сульфатов снизилось в сумме анионов на 10 %, что связано со снижением их количеств в воде в 3 раза и более (рис. 2). Отметим, что среднее содержание сульфатов в марте составляло 52 мг/л, в июле − 16 мг/л.
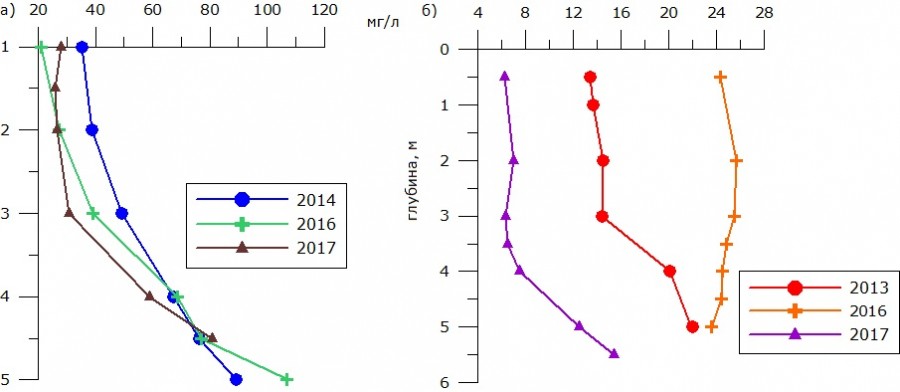
Рис. 2. Распределение сульфатов в водной толще оз. Назаровское а) в зимний и б) в летний периоды
Fig. 2. Distribution of sulfates in the water column of Lake Nazarovskoe a) in the winter and b) in the summer
Количество сульфатов ко дну постепенно увеличивается в 4‒5 раз (рис. 2а): подо льдом их концентрация изменялась от 21 до 35 мг/л (в среднем – 28.00 мг/л), в придонном горизонте − от 80 до 107 мг/л (89.12 мг/л). Это максимальное (на данном этапе исследований) количество сульфатов для данного озера. В летний период также отмечалось увеличение концентрации сульфатов ко дну, за исключением 2016 г. Лето 2017 г. было более дождливым по сравнению с предыдущими годами исследования, что сказалось и на количестве сульфатов – оно наименьшее за весь период исследований (рис. 2б). В поверхностном слое водной толщи концентрация сульфатов изменялась от 6 до 25 мг/л (в среднем – 21.21 ± 9.99 мг/л), в придонном слое − от 15 до 107 мг/л (49.83 ± 35.02 мг/л).
В марте среднее значение рН было 6.50, что свидетельствовало о некотором подкислении вод (минимальные значения показателя достигали 5.50), следовательно, при таких значениях рН больше 80 % сероводорода могло находиться в молекулярной форме (более токсичной для гидробионтов). В июле среднее значение составляло 7.45 (изменяясь от 7.10 до 8.12), в этих условиях он встречался в основном в форме гидросульфид-иона. Именно при наличии льда на озере определение сероводорода особенно необходимо.
Как зимой, так и летом поверхностные слои воды содержали кислород (от 3 до 9 мг/л). В марте, начиная с трех метров и до дна, наблюдается исчерпание кислорода (концентрация была чуть более 0 мг/л). В летний период в верхних слоях содержание кислорода составляло от 7 до 9 мг/л, затем постепенно происходило снижение его практически до нуля (минимум зафиксирован в придонном слое воды).
Среднее содержание растворенного органического углерода в марте составляло 27.26 ± 7.58 мг/л; в июле – 17.32 ± 1.29 мг/л.
Среднее содержание сероводорода/сульфидов зимой значительно превышало данные для летнего периода (рис. 3) и составляло 340, летом − 28 мкг/л. Для сравнения приведены полученные данные по содержанию этого соединения в воде соседнего с оз. Назаровское оз. Белое − в среднем 152 мкг/л и других изученных нами озер: Святое – 7 мкг/л, Нижнее – 11 мкг/л и Верхнее – 5 мкг/л (все водоемы расположены на территории Коношского района Архангельской области).
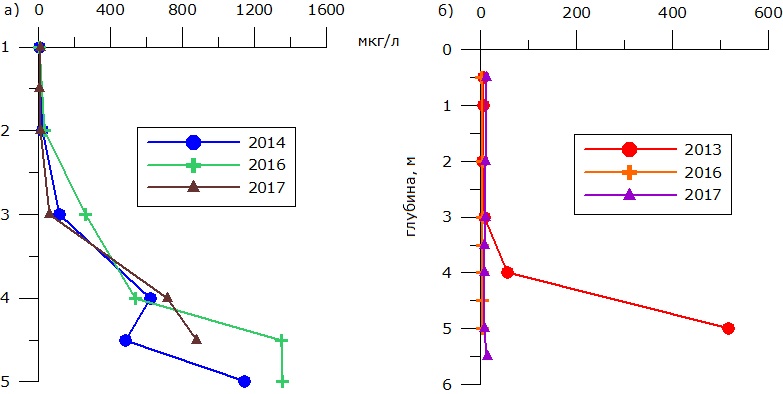
Рис. 3. Распределение сероводорода и сульфидов в водной толще оз. Назаровское а) в зимний и б) летний периоды
Fig. 3. Distribution of hydrogen sulfide and sulphides in the water column of Lake Nazarovskoe a) winter and b) summer periods
Поверхностный слой водной толщи содержал минимальные количества сероводорода/сульфидов – 5.91 ± 4.12 мкг/л, в придонном слое их содержится в 130 раз больше – 779 ± 548 мкг/л (максимум 1355 мкг/л). Концентрация сульфатов в придонном слое воды больше, чем на поверхности озера.
В летний период наблюдалось снижение концентрации сероводорода/сульфидов − в среднем до 28 мкг/л, максимум отмечен в 2013 г. − 517 мкг/л (среднее значение концентрации для оз. Белое составляло 12; оз. Святое – 10; оз. Нижнее – 37 (максимум 292); оз. Верхнее – 9 мкг/л). При этом в придонном слое водной толщи в летний период интенсивность процесса сульфатредукции была выше – 29.45 мкг S/дм3 сут, чем зимой, когда практически не наблюдалось протекание процесса, – 1.09 мкг S/дм3 сут.
Продуцирование сероводорода в ходе сульфатредукции и образование его производных соединений находит продолжение и в донных отложениях озер.
Содержание сульфатной серы (по применяемой методике параметр включает сульфаты жидкой и твердой фаз ДО) в среднем составляло 0.78 ± 0.72 % (в расчете на абсолютно сухое вещество).
В жидкой фазе осадков оз. Назаровское отмечено содержание сульфатов, в среднем в марте и июле превышающее 2500 мг/л. В марте их количество составляло в среднем 2850 мг/л, увеличиваясь от поверхностного слоя отложений в их толщу от 2300 до 3600 мг/л; в июле – 3180 мг/л, снижаясь незначительно по мере погружения в толщу отложений от 3100 до 2800 мг/л.
Не подвергшееся минерализации органическое вещество (в пересчете на органический углерод) сохранилось в донных отложениях в среднем количестве 9.50 % а.с.в., уменьшаясь к более глубоким слоям. Количество неизрасходованного лабильного ОВ составляло в поверхностном слое отложений в марте – 7.21 %, в июле – 6.18 %, что говорит о чуть большем его количестве в зимний период. Количество не подвергшегося минерализации органического вещества в ДО (в пересчете на углерод) в зимний период в среднем превышало его содержание летом. Доля лабильной фракции ОВ в июле насчитывала в оставшемся ОВ до 70 %.
Содержание железа в жидкой фазе ДО в марте изменялось от 120 до 240 мкг/л; в июле – от 250 до 510 мкг/л. В сумме твердой и жидкой фаз отложений восстановленная форма реакционноспособного железа (т. е. способного к переходу из одной фазы в другую при смене физико-химических условий в среде) содержалась в количестве 1.59 ± 0.74 % (в расчете на сухое вещество). Содержание железа в составе моносульфидов не превышало в среднем 0.02 %; пирита ‒ 0.61 %, изменяясь от 0.00 до 2.28 %. Эти величины говорят о различной интенсивности процесса сульфатредукции в отложениях, что привело к накоплению производных сероводорода в ДО также в разных количествах.
В ходе проведенных исследований было установлено, что среднее содержание соединений восстановленной серы в ДО оз. Назаровское с 2013 по 2017 годы составляло в марте 1.36 ± 0.88 % а.с.в., изменяясь в интервале от 0.13 до 3.14 %; в июле – 1.40 ± 1.00 % (от 0.08 до 3.96 %) (рис. 4).
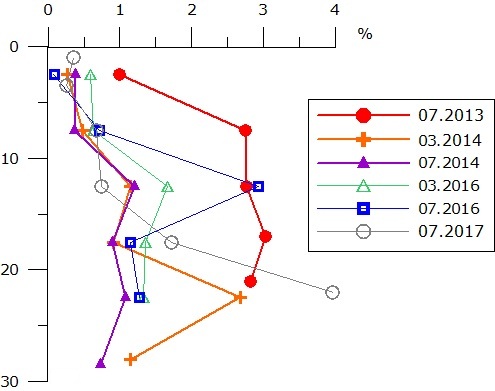
Рис. 4. Распределение соединений восстановленной серы в донных отложениях оз. Назаровское
Fig. 4. Distribution of reduced sulfur compounds in bottom sediments of Lake Nazarovskoe
Обсуждение
Полученные данные по гидрохимическим показателям (рН, содержание кислорода, растворенного органического углерода, сульфатов) оз. Назаровское свидетельствуют о создании в придонных слоях воды в оба сезона условий, которые не препятствуют протеканию процесса сульфатредукции.
Данные по содержанию соединений восстановленной серы в воде и ДО пресноводных озер немногочисленны и представлены в публикациях середины прошлого века, а при современной тенденции изучение сульфатредукции сводится к определению только скорости процесса и видового разнообразия серных бактерий. Поэтому проводится сравнение с ранее полученными нами результатами.
Лимитирующим содержанием сульфатов считают величины от 8 до 40−100 мкмоль/л (Holmer, Storkholm, 2001), т. е. приблизительно от 1 до 10 мг/л. Для жидкой фазы ДО оз. Назаровское эта величина составляла 2500 мг/л. Следовательно, концентрации сульфатов не должны сдерживать деятельность сульфатредуцирующих бактерий в ДО изучаемого нами озера.
В других исследованных нами водоемах концентрация сульфатов в жидкой ДО составляла: оз. Белое в среднем − 5280, оз. Нижнее − 496, оз. Святое – 1334 мг/л (Титова и др., 2017).
Величина ∑SH2S в донных отложениях других водоемов Коношского района составляла: оз. Белое – 2.40 % (от 0.00 до 8.94 %); оз. Нижнее – 0.19 % (от 0.04 до 1.12 %); оз. Святое – 0.29 % (от 0.04 до 3.18 %) (Титова и др., 2017).
При рассмотрении накопления соединений восстановленной серы только в годы, когда отбор проводился в оба сезона, содержание ∑SH2S будет выглядеть следующим образом: март – 1.64 ± 0.87 % (от 0.27 до 3.14 %), июль – 1.21 ± 0.73 % (от 0.08 до 2.94 %).
В табл. 1 приведено в среднем распределение форм в составе ∑SH2S в ДО оз. Назаровское.
Таблица 1. Распределение форм серы в составе ∑SH2S по сезонам в донных отложениях оз. Назаровское
Table 1. Distribution of sulfur forms in the composition ∑SH2S by seasons in bottom sediments of Lake Nazarovskoe
| % от ∑SH2S | Март | Июль |
| Сульфидная | 1.10 | 0.40 |
| Элементная | 1.49 | 1.03 |
| Пиритная | 40.46 | 52.59 |
| Органическая | 56.95 | 45.98 |
Из представленных выше данных видно, что пиритная сера среди соединений восстановленной серы преобладала или занимала последующее место в оба сезона, в донных отложениях пирит может образоваться только в результате преобразования образующегося сероводорода и сульфидов. Количества сульфидной серы в ДО озера минимальны. Наличие элементной серы, хотя и в небольших количествах, свидетельствует, что окисление сероводорода/сульфидов имело место в отложениях, но, возможно, эта форма также расходовалась при трансформации продуктов ОВ и при образовании пирита.
Содержание органической серы, доминирующей среди форм зимой, составляло − 1.04 % а.с.в., в летний период количество сокращалось почти вдвое − до 0.55 % а.с.в., уступая эту роль пириту − 0.66 % а.с.в. Следовательно, происходит сокращение количеств органической серы, которая могла служить в качестве дополнительного источника соединений серы (Rudd et al., 1986) (с последующим вовлечением последних в цикл этого элемента) при минерализации ОВ.
Для систематизации вышеописанных результатов они были обобщены в табл. 2.
Таблица 2. Сводные результаты показателей в воде и донных отложениях оз. Назаровское
Table 2. Summary results of indicators in water and bottom sediments of Lake Nazarovskoe
| Показатель | Март | Июль |
| Вода | ||
| рН | 6.50 | 7.45 |
| Кислород, мг/л | 0 | 5 |
| РОУ, мг/л | 27.26 | 17.32 |
| Сульфаты, мг/л | 52 | 16 |
| Сероводород/сульфиды, мкг/л (max) | 340 (1355) | 28 (152) |
| Донные отложения | ||
| Сульфаты, мг/л | 2850 | 3180 |
| Железо раств., мкг/л | 200 | 350 |
| Лабильное ОВ, %. | 7.21 | 6.18 |
| Железо пиритное, % | 0.58 | 0.65 |
| Сумма восстановленной серы, % | 1.64 | 1.21 |
Были изучены корреляционные зависимости между характеризующими протекание сульфатредукции и накопление соединений восстановленной серы показателями в образцах, отобранных в марте и июле одного и того же года.
Только для донных отложений (n = 20) отбора в марте отмечены обратные зависимости между содержанием органического вещества (Сорг) и следующими показателями (р < 0.05): S2- (-0.62), S пир (-0.52), Fe(II) (-0.52), SO42- (-0.75), что позволяет предположить протекание в осадках восстановительных процессов с затратой ОВ, в том числе и на процесс сульфатредукции. Для ДО отбора в июле (n = 19) не выявлено никаких явно выраженных зависимостей между этими же показателями.
Максимальная скорость изучаемого процесса установлена в летний период для поверхностных слоев ДО − до 555 мкг S/дм3 сут (для ДО оз. Белое этот показатель составлял около 2000 мкг S/дм3 сут), а в зимний период максимум отмечен для слоя 9−10 см − 338 мкг S/дм3 сут. Это может быть связано с тем, что в период осенней гомотермии и непосредственно летом происходит дополнительное поступление в ДО органического вещества со стоками с водосбора или в результате отмирания водорослей, растительности и водных организмов; проникновение кислорода в толщу отложений (до 15 см) и частичное окисление соединений восстановленной серы (приводящее к пополнению запаса сульфатов). В подледный период кислород в ДО заканчивается в результате расходования его на окислительные процессы ‒ условия постепенно сменяются сначала на микроаэрофильные, затем на анаэробные, т. е. создаются условия для активизации деятельности СРБ. В период весенней гомотермии и открытой воды образовавшиеся ранее и образующиеся летом восстановленные соединения серы (∑SH2S) в верхних слоях отложений могут подвергаться окислительным процессам, поэтому, несмотря на значительную интенсивность процесса сульфатредукции, летом в ДО не происходит столь же явно выраженного накопления соединений восстановленной серы, как зимой. Однако в более глубоких слоях отложений отмечено накопление восстановленной серы, несмотря на более низкую скорость процесса сульфатредукции − максимальное содержание ∑SH2S зафиксировано в июле 2017 г. для горизонта 20−24 см, при том что интенсивность процесса сульфатредукции для этого слоя отложений составляла только 43 мкг S/дм3 сут, и совсем немного отличалась от интенсивности процесса для придонного слоя воды.
Заключение
В заключение обобщены и приведены факторы или показатели, которые влияли на протекание процесса сульфатредукции и накопление соединений восстановленной серы в воде и донных отложениях оз. Назаровское, показаны особенности этих процессов.
По минерализации воды, составляющей в среднем 146 мг/л, оз. Назаровское относится к пресноводным водоемам. В зимний период это показатель практически вдвое выше, чем летом. По содержанию главных ионов − к категории гидрокарбонатного класса кальциевой группы. При этом среднее содержание сульфатов в воде данного водоема составляло 35 ± 25 мг/л, максимально − 106 мг/л. Представленные значения − наибольшие для всех изученных нами пресноводных озер. Несмотря на это, отмечено увеличение их количества зимой относительно летнего периода и от поверхности ко дну в оба сезона (несмотря на протекание сульфатредукции), что может косвенно свидетельствовать о поступлении сульфатов с грунтовыми водами.
Наибольшее количество сероводорода составляло 1355 мкг/л (представленная величина максимальна как для данного озера, так и для других исследованных нами пресноводных озер) и было отмечено в зимний период. Для большинства других водоемов этот показатель максимален в летний период.
Как и для всех изученных нами ранее пресноводных водоемов, в оз. Назаровском более интенсивно восстановление сульфатов в ДО осуществлялось в летний период (максимальная скорость процесса составляла 555 мкг S/дм3 сут), хотя в целом интенсивность этого процесса в ДО оз. Назаровское была меньше, чем во всех ранее исследованных озерах.
В отличие от большинства ранее исследованных нами озер, расположенных на территории Архангельской области, в ДО которых доминирующей формой являлась ‒ органическая, а среди сульфидных − сера моносульфидов, в оз. Назаровском в целом доминирующей формой серы была пиритная, доля которой порой достигала 94 % от общего количества соединений восстановленной серы.
На накопление восстановленных соединений серы в ДО оз. Назаровское оказало влияние содержание сульфатов в жидкой фазе и скорость протекания процесса: с одной стороны, ∑SH2S в среднем на порядок больше, чем для большинства исследованных нами ранее озер, но с другой стороны, в 2 раза меньше, чем в ДО оз. Белое, в котором скорость сульфатредукции оказалась в 4 раза выше. Даже несмотря на то, что оз. Белое мельче исследуемого нами водоема в 2 раза и доступного для СРБ ОВ в нем должно быть меньше, соединений восстановленной серы должно было бы накапливаться меньше.
На основании полученных результатов можно предположить, что запас ∑SH2S в донных отложениях создается в зимний период, а летом лишь пополняется. В зимний период образовавшиеся соединения восстановленной серы накапливаются (в водоеме отмечены анаэробные условия даже в водной толще). Летом же образовавшиеся ранее и образующиеся непосредственно в период наибольшей активности процесса в верхних слоях отложений соединения восстановленной серы могут подвергаться окислительным процессам из-за небольшой глубины озера.
Библиография
Агроклиматический справочник по Архангельской области . Л.: Гидрометеоиздат, 1961. 220 с.
Вайнштейн М. Б. Сульфатвосстанавливающие бактерии водоемов: экология и кластерирование (Обзор) // Прикладная биохимия и микробиология. 1996. Т. 32. № 1. С. 136‒143.
Волков И. И. Геохимия серы в осадках океана . М.: Наука, 1984. 272 с.
Волков И. И., Жабина Н. Н. Методы определения различных соединений серы в морских осадках // Химический анализ морских осадков / Под ред. Э. А. Остроумова. М.: Наука, 1980. С. 5‒27.
Гельман Н. Э., Терентьева Н. А., Шанина Т. М. Методы количественного органического элементного микроанализа . М.: Химия, 1987. 296 с.
Глобальный биогеохимический цикл серы и влияние на него деятельности человека / Под ред. акад. Г. К. Скрябина. М.: Наука, 1983. 424 с.
ГОСТ 17.1.5.01-80. Охрана природы. Гидросфера. Общие требования к отбору проб донных отложений водных объектов для анализа на загрязненность . Введен 1982−01−01. Переиздан 2002‒08‒01. М.: Изд-во стандартов СССР, 1980. 5 с.
ГОСТ Р 51592-2000. Вода. Общие требования к отбору проб . Введен впервые 2001‒07‒01. М., 2001. 48 с.
Драбкова В. Г., Сорокин И. Н. Озеро и его водосбор – единая природная система . Л.: Наука, 1979. 195 с.
Иванов М. В. Распространение и геохимическая деятельность бактерий в осадках океана . Т. 2. Геохимия донных осадков / Океанология. Химия океана. М.: Наука, 1979. С. 312‒349.
Кононец М. Ю., Пахомова С. В., Розанов А. Г., Проскурнин М. А. Определение растворенных форм железа в морской воде с помощью феррозина // Журнал аналитической химии. 2002. Т. 57. № 7. С. 704‒708.
Остроумов Э. А. Метод определения форм восстановленной серы в отложениях Черного моря // Труды Института океанологии АН СССР. 1953. Т. 7. С. 57‒69.
ПНД ф 14.1:2:4.132-98. Методика выполнения измерений массовой концентрации анионов: нитрита, нитрата, хлорида, фторида, сульфата и фосфата в пробах природной питьевой и сточной воды методом ионной хроматографии . М., 2008. 21 с.
РД 52.24.450-2010. Массовая концентрация сероводорода и сульфидов в водах. Методика выполнения измерений фотометрическим методом с N,N-диметил-n-фенилендиамином . Ростов н/Д: Росгидромет, 2010. 50 с.
Соколов В. С. Определение реакционноспособных форм железа и марганца в морских осадках // Химический анализ морских осадков / Под ред. Э. А. Остроумова. М.: Наука, 1980. С. 28‒41.
Тимофеева С. С., Ошаров А. Б., Бейм А. М. Экологическая химия сернистых соединений . Иркутск: Изд-во Иркутского ун-та, 1991. 134 с.
Титова К. В., Кокрятская Н. М. Соединения серы в озерах на территории Кенозерского национального парка (Каргопольский район, Архангельская область) // Вопросы естествознания. 2018. Науки о Земле. № 4 (18). С. 67‒74.
Титова К. В., Кокрятская Н. М., Жибарева Т. А. Процесс сульфатредукции в пресноводных озерах (Белое, Нижнее, Святое) Коношского района Архангельской области // Вестник МГОУ. Естественные науки. 2017. № 4. С. 123‒134. DOI: 10.18384/2310-7189-2017-4-123-134
Хатчинсон Д. Лимнология: Географические, физические и химические характеристики озер . М.: Прогресс, 1969. 592 с.
Holmer M., Storkholm P. Sulphate reduction and sulphur cycling in lake sediments: a review // Freshwater Biology. 2001. Vol. 46. Issue 4. Р. 431‒451.
ISO 8245:1999. Water quality – Guidelines for the determination of total organic carbon (TOC) and dissolved organic carbon (DOC). Geneva: International Organization of Standardization, 1999. 11 р.
Rovira P., Vallejo V. Ramon. Labile and recalcitrant pools of carbon and nitrogen in organic matter decomposing at different depths in soil: an acid hydrolysis approach // Geoderma. 2002. Vol. 107. P. 109‒141. DOI: 10.1016/S0016-706(01)00143-4
Rudd J. W. M., Kelly C. A., Furutani A. The role of sulfate reduction in long term accumulation of organic and inorganic sulfur in lake sediments // Limnol. Oceanogr. 1986. Vol. 31 (6). P. 1281‒1291.
Благодарности
Работа выполнена за счет средств Минобрнауки РФ проекта № АААА-А18-118012390167-1 «Изучение закономерностей биогеохимических процессов циклов хлора и серы в экосистемах Арктики и Субарктики под влиянием природных и техногенных факторов».






 © 2011 - 2026
© 2011 - 2026